2026.04.15
新一代活细胞实时动态成像及功能分析系统 CELLCYTE X,可实时追踪并分析球体生长状态与健康程度,为药物评估提供客观量化指标(往期文章:《CellCyte X 细胞球体分析软件让 3D 球体实验更科学、更轻松》)。
本文将展示 CELLCYTE X 在高通量实验场景中的应用实践,重点呈现其针对高稳定性、高重复性肿瘤球状体模型及细胞迁移模型的长期实时监测与多维度功能分析方案。研究以乳腺癌细胞系 MDA-MB-231 为研究对象,利用 3D 生物打印技术构建球状体与细胞迁移模型,通过 CELLCYTE X 活细胞成像系统,连续 5–9 天对模型进行非侵入式追踪监测,系统性对比 TeloCol®-10(重组人 Ⅰ 型胶原蛋白)与Matrigel(基底膜基质胶)两种细胞外基质(ECM)材料的生物学性能。
研究结果显示:TeloCol®-10 在维持3D肿瘤球状体的结构完整性与形态稳定性方面显著优于 Matrigel,且两者生长速率相当;此外,TeloCol®-10 批次间一致性高,不含肿瘤源性生长因子干扰,更适用于高通量生物打印及长期体外药物筛选。
研究背景:为何需要更稳定的 3D 细胞基质?
Matrigel 虽被视为 3D 细胞培养的“金标准”之一,但其成分复杂、批次差异显著,含有多种肿瘤源性生长因子,且力学性能调控性差、样本硬度不均一,在长期培养中易发生降解,液滴也易脱落。相比之下,胶原蛋白作为天然组织的主要成分,生物相容性优良,机械性能可调。其中,TeloCol®-10(含 95% I 型胶原蛋白与 5% III 型胶原蛋白)保留了胶原的端肽结构,交联更充分,刚度更高,接近乳腺癌基质的生理刚度为构建更具生理相关性的3D肿瘤模型提供了理想的基质平台。
实验设计:高通量生物打印 + 实时活细胞成像
1. 细胞与材料
细胞:mCherry 标记的 MDA‑MB‑231 乳腺癌细胞。
基质:TeloCol®-10(6 mg/mL 或 4 mg/mL)和 Matrigel(6 mg/mL 或 4 mg/mL)。
打印方式:采用定制生物分配器,在 96 孔板中打印 1 μL 细胞‑水凝胶混合液滴。
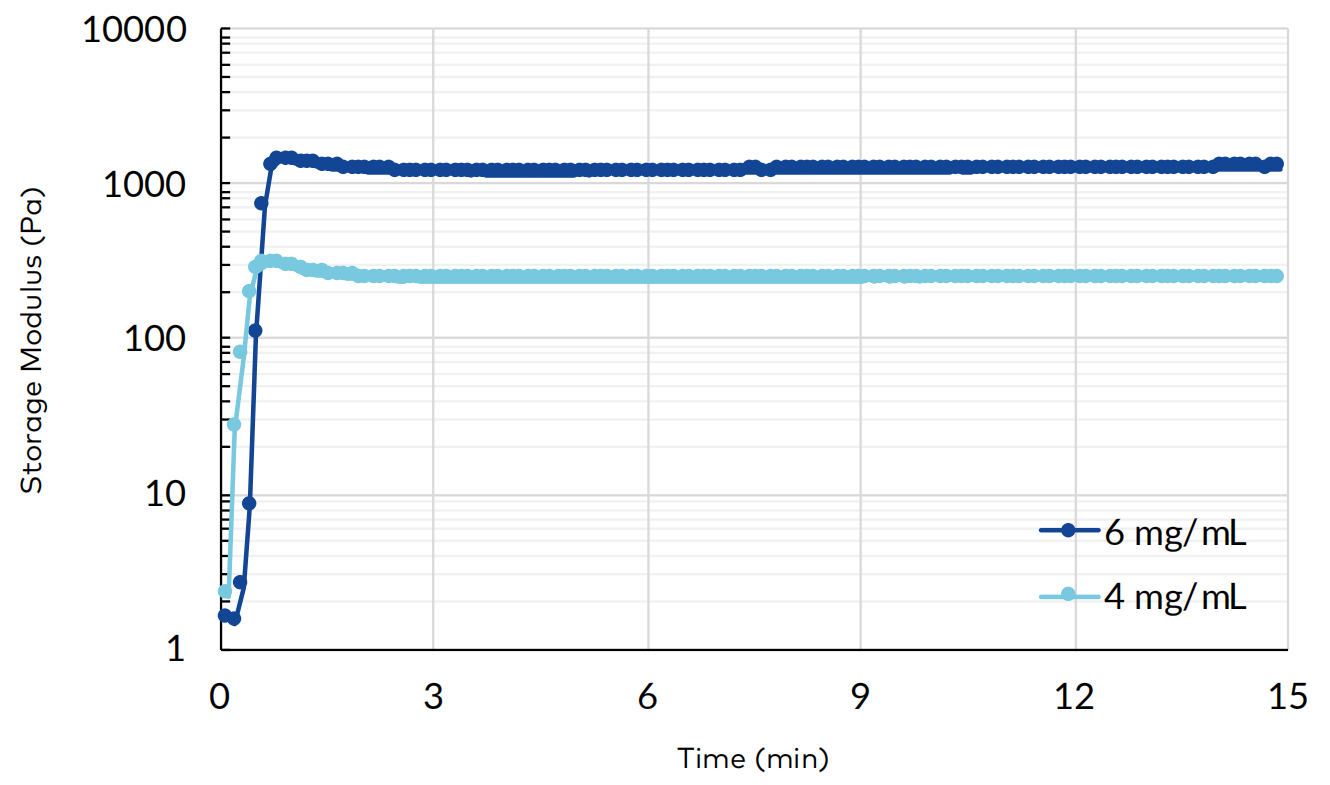
图1. TeloCol®-10稀释至6 mg/mL和4 mg/mL时的储存模量
2. 两种检测模型
球状体形成模型构建方法:将终浓度为 6 mg/mL的TeloCol®-10或Matrigel水凝胶与细胞悬液通过两支注射器反复推拉30次充分混匀,装入预冷至2℃的生物分配仪中,在96孔板内打印1 μL载细胞液滴,随后置于37℃培养箱中热交联(TeloCol®-10约15分钟,Matrigel约25分钟),每孔加入300 μL培养基,每3天半量换液,连续培养5天用于球状体形成观察。
细胞侵袭迁移模型(液滴嵌套式)构建方法:参照上述方法打印1 μL载细胞的内核液滴(6 mg/mL),经37℃交联后,在内核完全凝胶化的基础上,于其外层打印5 μL无细胞的4 mg/mL水凝胶以形成包裹结构,再次进行热交联,随后同样每孔加入300 μL培养基、每3天半量换液,连续培养9天以追踪细胞从内核向外层的侵袭迁移行为。
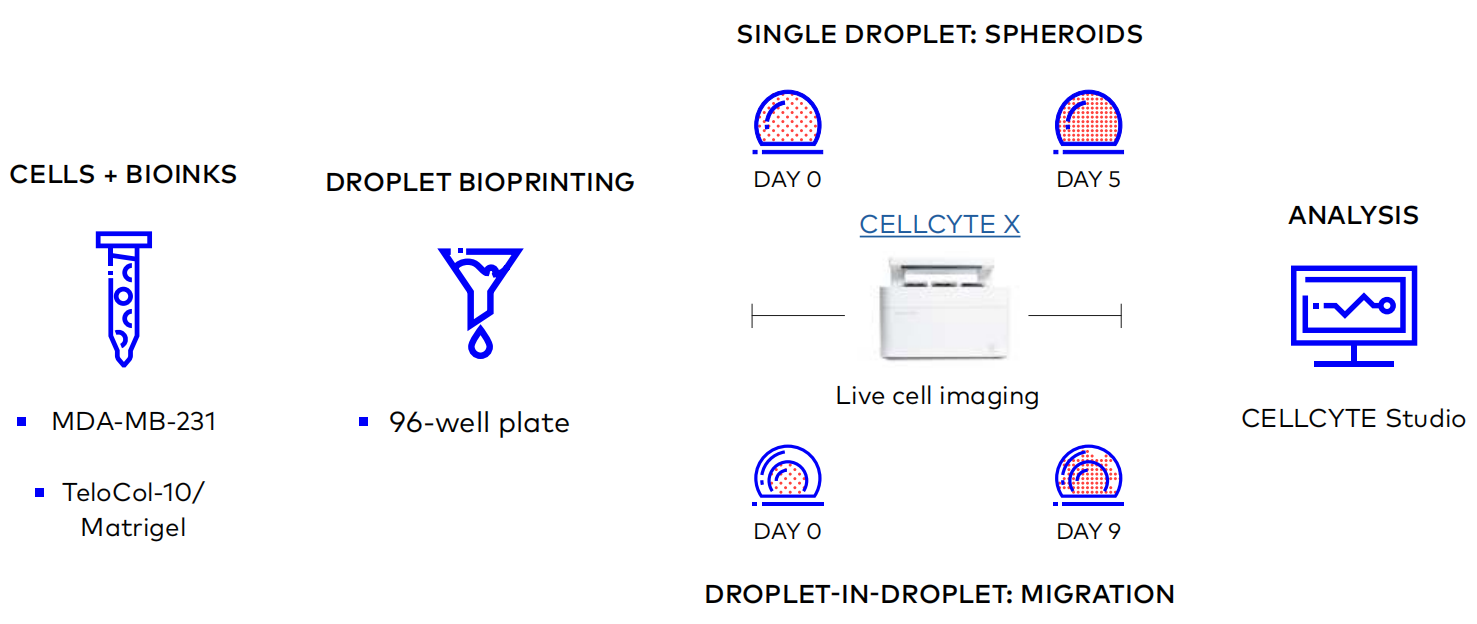
图2. TeloCol®-10/Matrigel 的球状体(液滴)与迁移模型(液滴嵌套式) 3D 生物打印及分析流程概览
3. 实时成像与定量分析
使用新一代活细胞实时动态成像及功能分析系统 CELLCYTE X,每 3 小时采集一次明场与红色荧光图像(4×物镜),连续监测 5–9 天,并借助系统自带的球体分析模块 CELLCYTE Studio,对总荧光强度进行归一化处理(Ft/Fi),量化细胞的生长与聚集情况。
实验结果:TeloCol®-10在稳定性上突出,Matrigel 易降解
✅ 球状体形成:两种基质均能支持球体形成,但稳定性差异显著
TeloCol®-10组:第 3 天开始聚集成团并形成类球体,持续生长至第 5 天(图 3A)。
Matrigel组:细胞第 2 天即形成类球体(图 3B)。第 3 天起,Matrigel液滴边缘开始降解,细胞团被推向孔板中央,部分细胞贴壁生长。第 4–5 天,小型类球体融合为大团簇,贴壁细胞过度生长占据孔底大部分区域。荧光监测显示,两组细胞生长速率一致(图 4)。
本结果证实 TeloCol®-10 在此体系中稳定性更优。

图3. TeloCol®-10 与 Matrigel 中 MDA-MB-231 球状体形成及降解对比
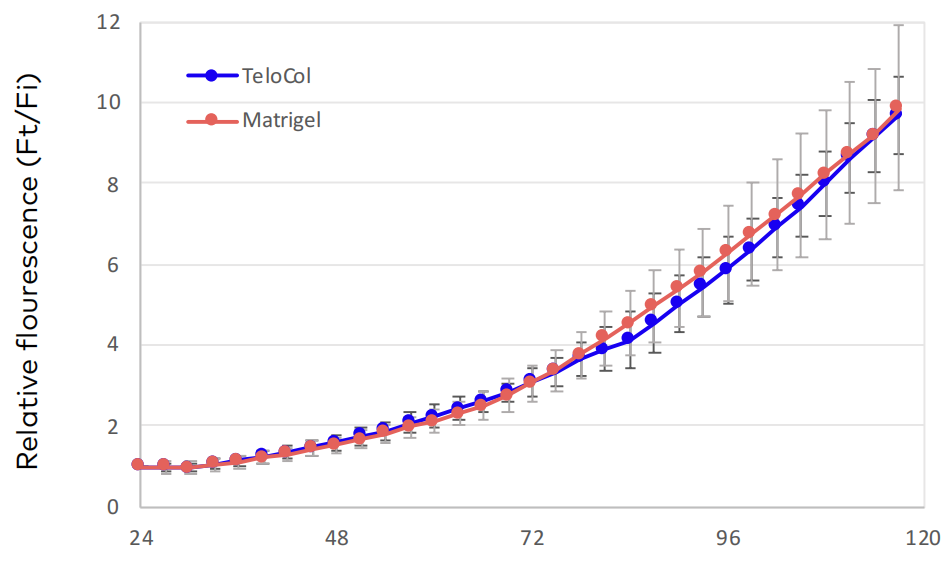
图4. 相对荧光强度显示 TeloCol®-10 与 Matrigel 中细胞增殖速率基本一致
✅ 迁移模型:TeloCol®-10可维持完整结构长达 7 天以上
TeloCol®-10组 与Matrigel组细胞均在第 3 天开始从内核向外层迁移,后续几天大量迁移。伴随细胞迁出,内核层降解,中央形成类球体团,与类球体模型中降解现象一致。第 7 天,Matrigel组外层开始降解收缩,向中央聚集,孔底留下细胞迁移轨迹。总体而言,TeloCol®-10组模型可连续监测迁移至第 9 天;Matrigel组模型细胞第 7 天已迁移至外层边缘(图5)。
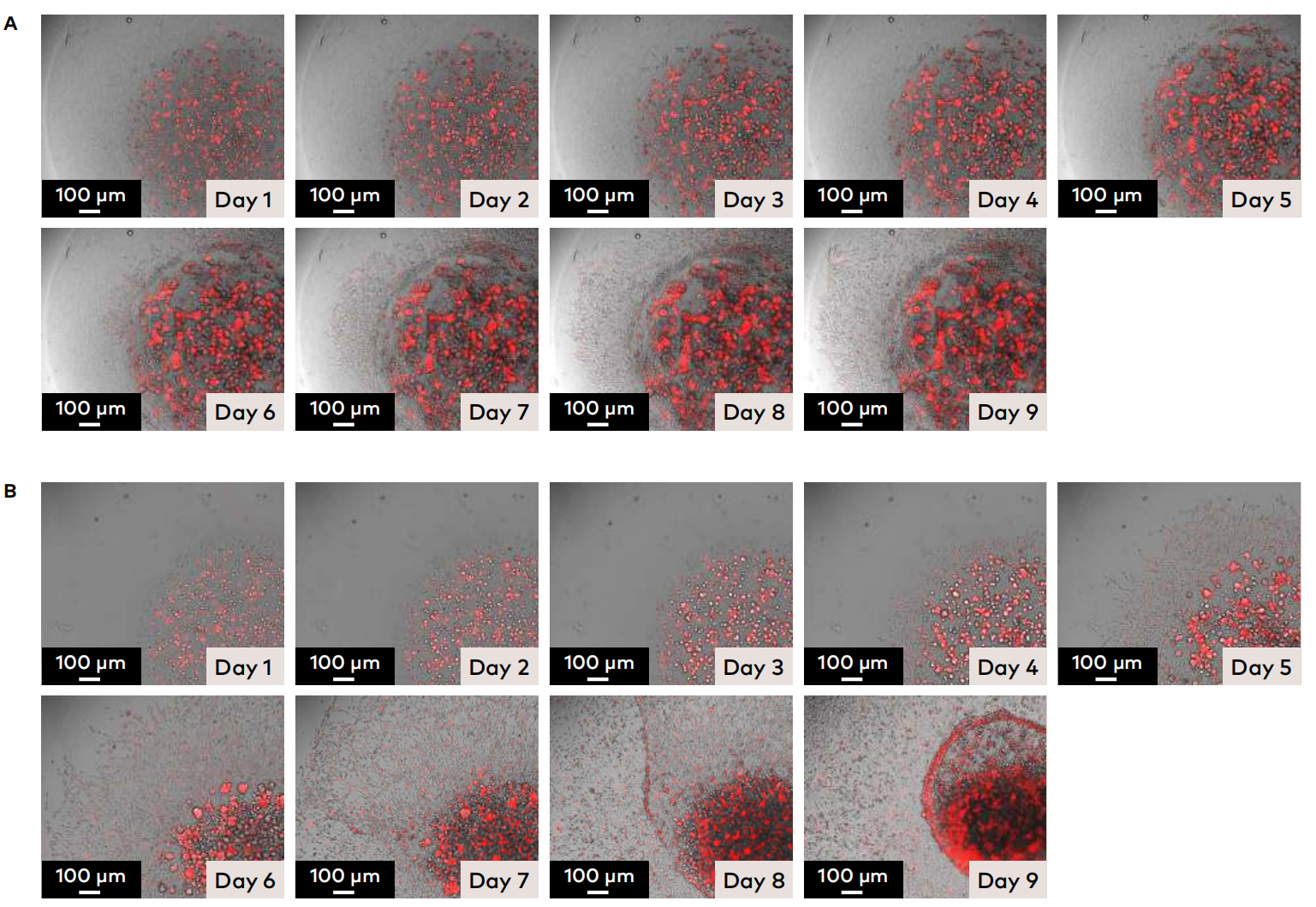
图5. TeloCol®-10 与 Matrigel 中的液滴嵌套式迁移模型对比(9天动态监测)
✅ Matrigel 易降解的核心原因
类球体与迁移实验中观察到的Matrigel 降解,与生长细胞的蛋白水解作用相关。1 μL 小体积液滴、4–6 mg/mL 浓度、高细胞密度均可能加剧降解。薄层的Matrigel 易形成异常结构,细胞倾向于单层生长。此外,Matrigel 蛋白与生长因子组成的差异会影响凝胶力学性能、细胞生长、迁移与实验重复性。前期实验显示,换液或加药时Matrigel液滴易从孔底脱落;而 TeloCol®-10液滴可稳定黏附于孔中央。
实验结论:TeloCol®‑10 是高通量 3D 生物打印的更优选择
在相同浓度下,TeloCol®-10 与 Matrigel 均能支持乳腺癌细胞的球状体形成与迁移,且细胞生长速率基本一致。然而,Matrigel 在球状体模型中培养 4 天后即出现明显降解,在迁移模型中于第 6–7 天也发生降解;相比之下,TeloCol®-10因保留端肽结构而具有更高的刚度(1.2 kPa)和超过 99% 的纯度,在整个实验周期内未出现任何降解迹象。同时,TeloCol®-10 不含 Matrigel 中复杂的生长因子及批次差异,因此更适用于高通量生物打印与长期药物筛选等应用场景。
CELLCYTE X 在此次研究中发挥了关键作用:
高通量:支持 96 孔板全自动并行监测,适配大规模筛选需求;
长时程:实现原位培养与连续成像,全程不干扰细胞正常状态;
定量化:内置球状体分析模块,可快速完成对细胞聚集、迁移及生长过程的量化评估。
未来展望
本研究通过 3D 生物打印结合 CELLCYTE X 活细胞实时成像系统,成功构建高通量乳腺癌细胞球状体形成与迁移模型,并通过多维度验证了TeloCol®-10相较于 Matrigel 在 3D 细胞培养中的优势。而 CELLCYTE X 凭借高通量并行监测、长时程非侵入式追踪及多参数精准量化分析技术,为3D模型的构建质控、动态行为监测及实验数据的客观评估提供了核心技术支撑,二者结合为肿瘤生物学研究、体外药物筛选与高通量 3D 生物打印模型开发,提供了更稳定、可重复、更贴近生理环境的高效解决方案。




